
上海研倍新材料科技有限公司
 白金会员
白金会员 已认证
已认证

上海研倍新材料科技有限公司
 白金会员
白金会员 已认证
已认证

类器官(Organoids)是由干细胞通过自组织形成的三维微观器官模型,能够模拟真实器官的结构与功能,在疾病建模、药物筛选和再生医学中展现出巨大潜力。然而,传统类器官构建依赖细胞因子和小分子化合物,存在成本高、批次差异大等问题。
纳米材料是指至少有一维处于纳米尺度(1 - 100nm)的材料,具有独特的光学、磁学和电学等性质,在癌症治疗、药物递送和成像等方面已取得显著进展。近年来,纳米材料与纳米技术的引入为类器官研究开辟了新路径,不仅优化了培养体系,还推动了其在个性化医疗中的应用。本文基于《ACS Nano》2024年的综述,系统解析纳米材料如何调控干细胞命运、构建三维微环境,并探讨其在精准医疗中的前景与挑战。
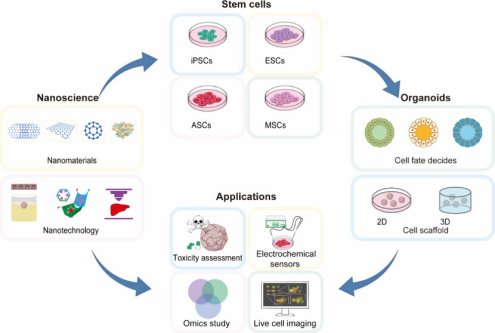
干细胞的分化受生物化学信号(如细胞因子)和物理信号(机械、电、磁等)共同调控。纳米材料凭借其独特的物理化学性质,成为调控干细胞命运的“智能工具”。
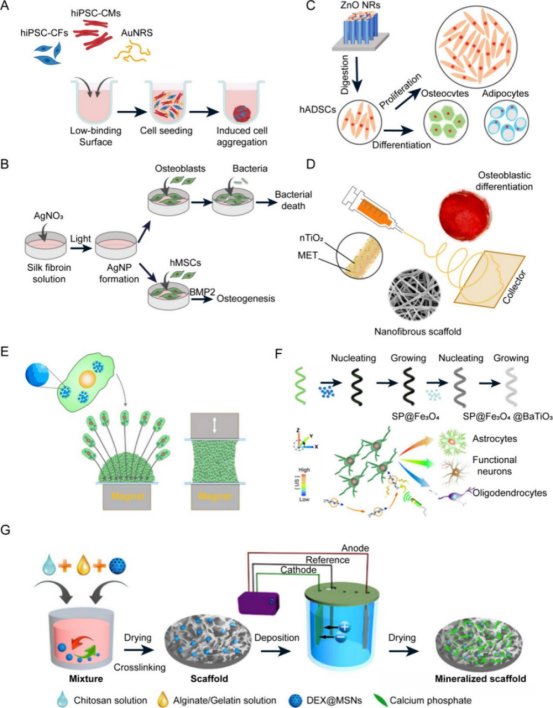
金纳米颗粒(AuNPs):通过表面功能化递送神经营养因子,促进脑类器官成熟。电磁场激活的金纳米颗粒可上调组蛋白乙酰化,加速神经元分化。
银纳米颗粒(AgNPs):具有抗菌特性,但其高浓度可能诱导脑类器官的神经发育毒性,需严格控制剂量。
磁性纳米颗粒(MNPs):结合磁场远程操控胚胎干细胞聚集成三维拟胚体,定向分化为心肌细胞。例如,Fe3O₄纳米颗粒通过磁拉伸驱动干细胞向中胚层分化。
碳纳米管(CNTs):嵌入胚胎体(EBs)中提升电导率,促进心肌分化;垂直排列的CNT阵列模拟细胞外基质(ECM),支持神经干细胞分化为功能性神经元。
石墨烯及其衍生物:石墨烯氧化物(GO)通过激活Wnt/β-catenin通路促进骨髓间充质干细胞的成骨分化;导电石墨烯薄膜结合无线电磁刺激,诱导脂肪干细胞分化为神经元。
案例:Patino-Guerrero团队将金纳米棒(AuNRs)与心脏类器官共培养,显著上调心肌标志基因(如MYH6、TNNT2),证明纳米材料可增强类器官功能与成熟度。
传统类器官培养依赖基质胶(如Matrigel),但缺乏血管化和营养传输能力。纳米技术通过以下策略优化三维微环境:
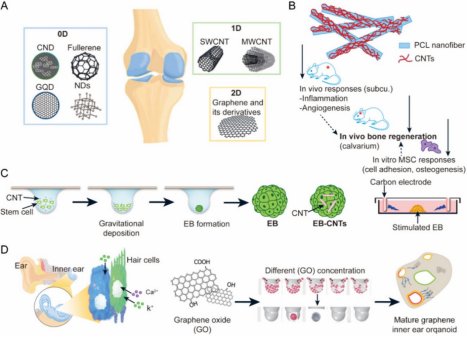
DNA水凝胶:通过自组装形成动态交联网络,支持多能干细胞高效增殖与形态发生。例如,DyNAtrix合成水凝胶成功构建胎盘类器官,模拟体内发育过程。
磁性纳米颗粒标记的细胞在磁场中悬浮,形成均一球体。该技术无需支架,避免材料干扰,已用于脂肪组织类器官和骨细胞球体的构建,重现组织异质性。
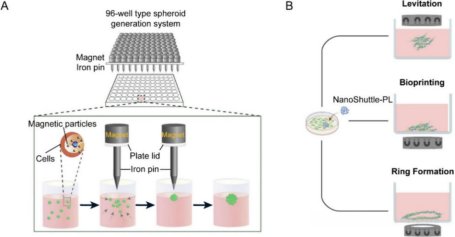
纳米复合生物墨水(如明胶-纳米羟基磷灰石)结合光固化技术,打印出具有复杂结构的类器官支架。例如,载超顺磁氧化铁(USPIO)的胆管支架可通过MRI实时监测修复过程。
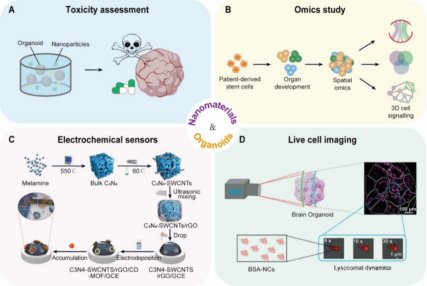
类器官模拟器官特异性反应,用于纳米材料安全性评价。例如,人肠道类器官暴露于纳米塑料后,显示剂量依赖性通透性增加和绒毛损伤,揭示其潜在健康风险。
纳米探针结合质谱/转录组技术,揭示石墨烯氧化物(GO)通过内质网应激扰乱脑类器官脂代谢,为神经退行性疾病研究提供线索。
金纳米棒光学传感器实时追踪胰岛类器官的胰岛素分泌;碳纳米管电极阵列无创记录脑类器官的神经电活动,推动高通量药物筛选。
近红外荧光纳米探针(如HD-Br)实现肝类器官溶酶体超分辨成像;贵金属纳米簇标记脑类器官,动态观察亚细胞器活动。
生物相容性与标准化:需系统评估纳米材料的长期毒性,建立制备与表征的国际标准。
替代细胞因子:开发通过物理信号(如光、磁)调控干细胞分化的纳米材料,降低对昂贵生长因子的依赖。
血管化与规模化:结合微流控和纳米纤维技术,构建血管化类器官,提升营养传输与药物测试效率。
临床转化:推动纳米类器官模型在个体化治疗方案设计中的应用,例如肿瘤患者药敏测试或器官移植前评估。
纳米材料与类器官的交叉融合,正重塑生物医学研究的范式。从精准调控干细胞到构建仿生微环境,纳米技术不仅解决了传统类器官的局限性,还为其在毒性评估、疾病建模和个性化治疗中的应用注入新动能。未来,随着材料科学与生物工程的深度协同,这一领域有望实现从实验室到临床的跨越,为人类健康带来革命性突破。
本文基于ACS Nano 2024综述《Nanomaterials in Organoids: From Interactions to Personalized》
相关产品
更多
相关文章
更多
技术文章
2026-03-05技术文章
2025-11-06技术文章
2025-08-11技术文章
2025-08-02
请拨打厂商400电话进行咨询
使用微信扫码拨号